02 – OTIMIZAÇÃO DA SÍNTESE DE ANALCIMA ‘CONDICIONADOR DE SOLO’ A PARTIR DE REJEITO GIBBSÍTICO-CAULINÍTICO DERIVADO DE BAUXITA: UMA ANÁLISE DE DRX-CLUSTER ASSOCIADA A UMA MATRIZ DOE
Ano 10 (2023) – Número 1 - Agrominerais Artigos
![]() 10.31419/ISSN.2594-942X.v102023i1agromineraisa2LVOM
10.31419/ISSN.2594-942X.v102023i1agromineraisa2LVOM
SYNTHESIS OPTIMIZATION OF ANALCIME ‘SOIL CONDITIONER’ DERIVATED FROM GIBBSITE-KAOLINITE WASTE BAUXITE: AN XRD- CLUSTER ANALYSIS ASSOCIATED WITH A DOE MATRIX
Luan V. O. Mourão*1
Andréia O. Rodrigues2
Rômulo S. Angélica2
Simone P. A. Paz1,2
1Faculdade de Engenharia Química, Instituto de Tecnologia, Universidade Federal do Pará (UFPA), Belém, Pará, Brasil, luan.mourao@itec.ufpa.br*1
2Laboratório de Caracterização Mineral (LCM), Instituto de Geociências, UFPA, Belém, Pará, Brasil.
*Autor correspondente
ABSTRACT
The main objective of this work was to use the XRD-Cluster analysis associated with a 23 full factorial design of experiments to optimize the synthesis process of analcime (a zeolite used as soil conditioner) from gibbsite-kaolinite waste from bauxite beneficiation combined with the siliceous co-product of silicon metal production (amorphous silica). The variables included the NaOH solution concentration (1.5-3.5 M), temperature (110-180 ºC) and time (4-48 hours). Concentration is the most important variable and according to the clusters formed, it can be said that the optimal conditions are: NaOH solution concentration of 2.5 M; temperature of 145 ºC and time of 26 hours.
Keywords: Zeolite; Principal Component Analysis (PCA); multivariate statistics.
1. INTRODUÇÃO
No Brasil, o setor mineral tem uma enorme importância no cenário econômico, com destaque singular para o estado do Pará, principalmente na cadeia minerometalúrgica de Bauxita-Alumina-Alumínio. As principais empresas que produzem bauxita lavada nesta região são: Mineração Rio do Norte (MRN), a mais antiga em operação, desde o final dos anos 70; Hydro Mineração Paragominas, iniciada em 2007 e Aluminum Company of America (ALCOA), iniciada em 2009 (Paz, 2016; Paz et al., 2017a; 2017b; Paz et al., 2018; Angélica et al., 2018). De acordo com o sumário mineral 2018, do Departamento Nacional de Produção Mineral (Brasil, 2018), a produção de bauxita, apenas dessas três empresas (MRN, Hydro e ALCOA), alcançou cerca de 36 Mt, o que representa mais de 85% da produção brasileira.
O beneficiamento da bauxita amazônica (classificação a úmido conhecido por lavagem) é realizado para liberar o mineral de interesse (gibbsita) do mineral de ganga (caulinita). Neste processo, a recuperação tem variado, de maneira geral, entre 60-80 % e o rejeito rico em gibbsita e caulinita armazenado em grandes e onerosas lagoas e/ou bacias de sedimentação (Nascimento et al., 2013; Paz, 2016; Paz et al., 2018; Angélica et al., 2018; Melo et al., 2019).
As bauxitas de Paragominas, nordeste do Estado do Pará, apresentam elevado conteúdo caulinítico, e por isso muitas de suas variedades são classificadas como bauxitas marginais ou estéreis. Assim, durante o beneficiamento, faz-se necessário operações de desagregação/lavagem para liberar o mineral gibbsita do argilomineral caulinita, esse conhecido na minerometalurgia do alumínio como sílica reativa e, por isso, também considerado deletério. Devido à relação textural de intercrescimento entre os cristais desses dois minerais, muita gibbsita é perdida neste processo, o que resulta em um rejeito com altos teores de caulinita e gibbsita (Nascimento et al., 2013; Paz, 2016; Paz et al., 2017a; 2017b; Paz et al., 2018; Angélica et al., 2018; Melo et al., 2019).
O rejeito proveniente do beneficiamento de bauxitas amazônicas possui em sua composição a gibbsita [γ-Al (OH)3], que é o mineral de alumínio mais comum nas bauxitas brasileiras e o mais desejado para o processo de extração metalúrgica via processo Bayer. Além disso, também há a presença de caulinita [Al2Si2O5(OH)4], um aluminossilicato comum em solos e lateritas-bauxitas. Ambos podem ser utilizados como fontes de alumínio e silício, respectivamente, para a síntese de materiais zeolíticos.
Zeólitas são aluminossilicatos, conhecidos como “peneiras moleculares”, com arranjo estrutural composto por um framework formado pela combinação tridimensional de tetraedros de AlO4 e SiO4, unidos entre si por ligações entre átomos de oxigênio. Sua estrutura apresenta canais e cavidades, nas quais se encontram moléculas de água e cátions trocáveis. Devido às suas particularidades estruturais, estes materiais possuem propriedades físico-químicas que tornam possível a sua aplicação para fins agrícolas, devido às suas propriedades de capacidade de troca catiônica (CTC), capacidade de retenção de água nos canais livres e também adsorção (Luz, 1995; Baerlocher et al., 2001; Bernardi et al., 2008; Bernardi et al., 2009a; 2009b; Paz et al., 2010; Pinheiro et al., 2021).
O nome da zeólita tipo analcima deriva do termo grego “an alkimos”, que significa “não forte”, em alusão à fraca energia eletrostática exibida por este mineral. Quimicamente é um silicato de alumínio e sódio hidratado, expresso comumente pela fórmula: Na16[(AlO2)16(SiO2)32].16H2O ou 8Na2O.8Al2O3.32SiO2.16H2O, e estruturalmente, suas cavidades e canais irregulares são ocupados por moléculas de água e sódio trocável, esse compensador de carga negativa gerada pelas substituições isomórficas de Si4+ por Al3+, nos sítios tetraédricos; além disso, seus canais não se cruzam. A obtenção deste mineral sinteticamente irá depender da razão SiO2/Al2O3 (geralmente varia em uma faixa de 1,5-3,0) e das condições físico-químicas de: temperatura, pressão, concentração da solução de NaOH e tempo (Bortolini et al., 2020; Menciá et al., 2020; Jin et al., 2022).
Diversos trabalhos já foram realizados no Brasil usando rejeitos minerais como fontes de silício e alumínio na síntese de zeólitas, dentre os quais destaca-se os realizados pelos Grupos de Mineralogia e Geoquímica Aplicada (GMGA) e Ciência e Engenharia Mineral (GCEM), ambos da Universidade Federal do Pará (Maia et al., 2007; Saldanha, 2007; Paz et al., 2010; Hildebrando, 2012; Nascimento et al., 2013; Menezes et al., 2017; Melo et al., 2019; Pinheiro et al., 2021).
Ao longo dos anos, a síntese de zeólitas sofreu uma grande evolução, não só no âmbito acadêmico, como também industrial, uma vez que este material pode ser modificado quimicamente para favorecer determinadas características, como por exemplo a capacidade de trocas catiônicas, o que possibilita o uso de zeólitas na agricultura como fertilizantes de liberação lenta e/ou condicionantes de solo (Bernardi et al., 2008; Bernardi et al., 2009a; 2009b).
Muitos dos trabalhos citados anteriormente sobre síntese de zeólitas foram desenvolvidos aplicando planejamento experimental do tipo uma variável por vez. No entanto, há a possibilidade de desenvolver e/ou otimizar processos aplicando estatística multivariada, isto é, analisar simultaneamente um conjunto de variáveis que caracterizam uma população ou amostra, a exemplos temos o planejamento experimental fatorial (DOE) e a análise de cluster (Box et al., 2005; Montgomery, 2008; Melo et al., 2019; Butler et al., 2020; Pinheiro et al., 2021).
Neste contexto, buscou-se otimizar o processo de síntese de analcima (zeólita usada para condicionar o solo) a partir do rejeito gibbsítico-caulinítico do beneficiamento de bauxita combinado com o coproduto silicoso da produção de silício metálico. Para tal, foi realizado uma análise de DRX-cluster associada a um planejamento experimental fatorial completo 23.
2. MATERIAIS E MÉTODOS
2.1 MATERIAIS
Os materiais de partida utilizados como fontes de silício e alumínio neste trabalho foram: rejeito gibbsítico-caulinítico proveniente da Mineração Paragominas SA – Norsk Hydro e um coproduto silicoso (sílica amorfa) produzido pela Dow Corning Metais do Pará. As nomenclaturas empregadas aos materiais de partida são apresentadas na Tabela 1, assim como a procedência. Além disso, foi utilizado hidróxido de sódio como fonte extra de sódio.
Tabela 1 – Procedência e identificação dos materiais.
| Material | Sigla | Procedência |
| Rejeito Gibbsítico-Caulinítico | RGC | Paragominas – PA |
| Sílica amorfa | SILMIX | Breu Branco – PA |
2.2. MÉTODOS
2.2.1. Preparação dos materiais de partida
Uma quantidade de 5 kg de cada material, RGC e SILMIX, foram homogeneizados e quarteados pelo método de pilha alongada com retomada das pontas, de onde foram amostradas uma quantidade de 200 g para ensaios de síntese e caracterização. A desagregação-homogeneização do RGC e SILMIX foi realizada por pulverização em almofariz de ágata Retsch, modelo RM 200.
2.2.2. Síntese hidrotermal
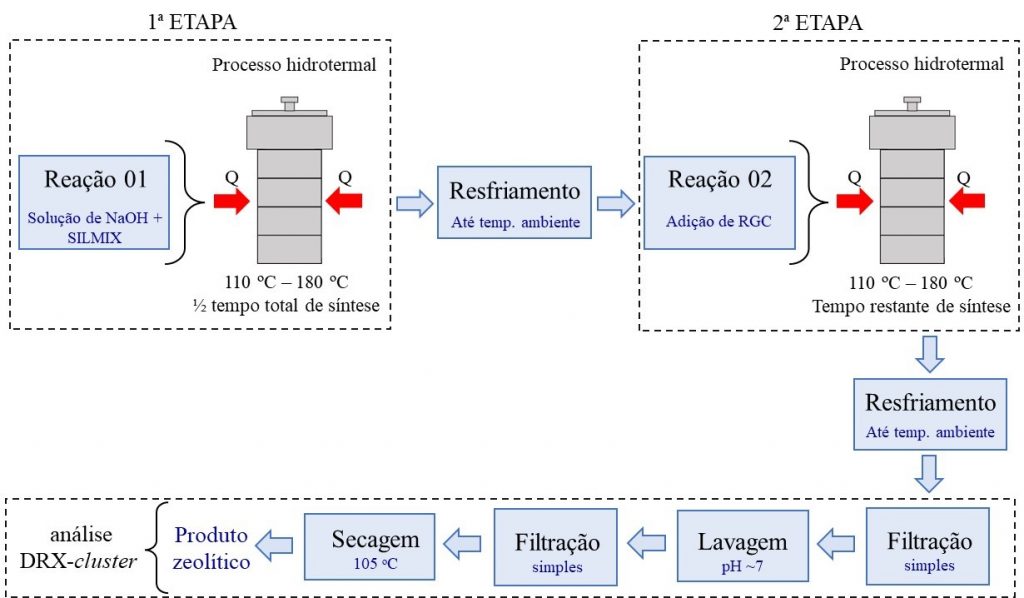
O processo de síntese mineral foi realizado em duas etapas: 1) Adicionou-se 2,32 g de SILMIX a 25 ml de solução de hidróxido de sódio (1,5-3,5 mol.L-1), em reatores de aço inoxidável com capacidade de 50 ml. O sistema foi devidamente homogeneizado e colocado em bloco digestor para reagir 1/2 do tempo total de síntese; 2) Os reatores foram resfriados em água corrente e receberam mais 0,78 g de RGC. O sistema foi homogeneizado e colocado no bloco digestor para reagir o restante do tempo total de síntese. Em seguida, os reatores foram resfriados até temperatura ambiente, a suspensão filtrada e lavada com água destilada até pH ~7. Finalmente, o produto foi seco em estufa a 105 ºC por 24 h (Fig. 1). Ver também o planejamento experimental fatorial completo 23 na seção 2.2.3, Tabelas 2 e 3.
2.2.3. Análises
Difratometria de raios X (DRX): Identificação de fases e análise de cluster
As medidas foram realizadas em um difratômetro de raios X, modelo EMPYREAN da PANalytical, com goniômetro θ-θ, tubo de raios X cerâmico e anodo de Co (Kα1 = 1,789010 Å), com foco fino longo, e filtro Kβ de Fe. O detector utilizado foi de área, do tipo PIXel3D 2×2, com abertura (active length) de 3,3473º 2θ e 255 canais ativos.
As condições de análise foram as seguintes: varredura de 5° a 75° 2θ; voltagem de 40 kV e corrente de 35 mA; tamanho de passo de 0,02º 2θ e 30s o tempo/passo; fenda divergente de 1/4° e antiespalhamento de 1/2°; máscara de 10mm. A aquisição de dados foi feita com o software X’Pert Data Collector e o tratamento dos dados com o software X´Pert HighScore, ambos da PANalytical.
Os parâmetros de comparação usados na análise de Cluster foram:
- “profile” + “peaks” como fonte de dados;
- Posição como um tipo de comparação com um “threshold” de 75%;
- “Euclidean” como distância de medida;
- “Average linkage” como método de ligação;
- Mínimo de cristalinidade igual a 5%;
- Manual “cut-off” de 36,7%.
Espectrometria de fluorescência de raios X (FRX)
A determinação da composição química foi realizada por espectrometria de fluorescência de raios X, utilizando um espectrômetro WDS sequencial, modelo Axios Minerals da marca PANalytical, com tubo de raios X cerâmico, anodo de ródio e máximo nível de potência 2,4W. A amostra foi analisada em disco fundido: 1 g de amostra + 6 g de fundente (Tetraborato de Lítio – Li2B4O7), mistura fundida a 1000 °C por 10 min. As aquisições e tratamento dos dados foram realizados através do software SuperQ Manager da PANalytical.
A perda ao fogo (P.F.) foi determinada por diferença de massas após calcinação da amostra a 1000 ºC por 1 hora (1 g da amostra previamente seca a 105 °C).
Planejamento Experimental Fatorial completo 23 (DOE)
Para esse estudo foi escolhido um planejamento fatorial completo 23, em que as três variáveis foram aquelas mais significativas para a síntese hidrotermal de zeólita analcima, baseado em trabalhos anteriores (Moraes et al., 2013; Bortolini et al., 2020; Menciá et al., 2020), são elas: concentração da solução de NaOH, temperatura e tempo, ver Tabela 2. Na Tabela 3, tem-se a matriz do planejamento em ordem padrão, com destaque para a ordem de realização dos ensaios. A ordem dos ensaios foi determinada por meio de sorteio para se obter uma aleatoriedade na realização dos experimentos. A resposta utilizada para a análise estatística do produto zeolítico foi o difratograma de raios X completo.
Tabela 2 – Variáveis e Níveis para o planejamento experimental fatorial completo 23.
| Variáveis codificadas | Variáveis Originais | Níveis | ||
| -1 | 0 | 1 | ||
| X1 | Concentração de NaOH (mol.L-1) | 1,5 | 2,5 | 3,5 |
| X2 | Temperatura (ºC) | 110 | 145 | 180 |
| X3 | Tempo (h) | 4 | 26 | 48 |
Tabela 3 – Matriz do planejamento experimental fatorial completo 23.
| Ensaios | Variáveis Codificadas | Variáveis Originais | ||||
| Ordem Padrão | X1 | X2 | X3 | mol.L-1 | ºC | h |
| ANA1(2) | – | – | – | 1,5 | 110 | 4 |
| ANA2(5) | + | – | – | 3,5 | 110 | 4 |
| ANA3(5) | – | + | – | 1,5 | 180 | 4 |
| ANA4(4) | + | + | – | 3,5 | 180 | 4 |
| ANA5(8) | – | – | + | 1,5 | 110 | 48 |
| ANA6(10) | + | – | + | 3,5 | 110 | 48 |
| ANA7(6) | – | + | + | 1,5 | 180 | 48 |
| ANA8(7) | + | + | + | 3,5 | 180 | 48 |
| ANA9(3) | 0 | 0 | 0 | 2,5 | 145 | 26 |
| ANA10(9) | 0 | 0 | 0 | 2,5 | 145 | 26 |
| ANA11(1) | 0 | 0 | 0 | 2,5 | 145 | 26 |
(*) Ordem de ensaio
3. RESULTADOS E DISCUSSÃO
3.1 CARACTERIZAÇÃO DOS MATERIAIS DE PARTIDA
A Fig. 2 apresenta o difratograma de raios X do rejeito gibbsítico-caulinítico. Verifica-se que o mesmo é composto essencialmente pelos minerais gibbsita e caulinita, como pode ser observado pelos seus picos principais (d002 = 4,85 Å e d100 = 4,37 Å) e (d001 = 7,15 Å e d002 = 3,57 Å), respectivamente. Verifica-se ainda, a presença de anatásio (d101 = 3,52 Å), hematita (d104 = 2,69 Å) e goethita aluminosa (d110 = 4,12 Å).
No trabalho realizado por Nascimento et al. (2013), os autores quantificaram o material RGC que apresentou valor médio (n=3) para gibbsita e caulinita de 47,92% ± 0,23 e 32,27% ± 0,85, respectivamente. De acordo com Melo et al. (2019), tais informações confirmam a expectativa de que este material seja uma boa fonte de Al2O3 e SiO2 para a produção de zeólitas.
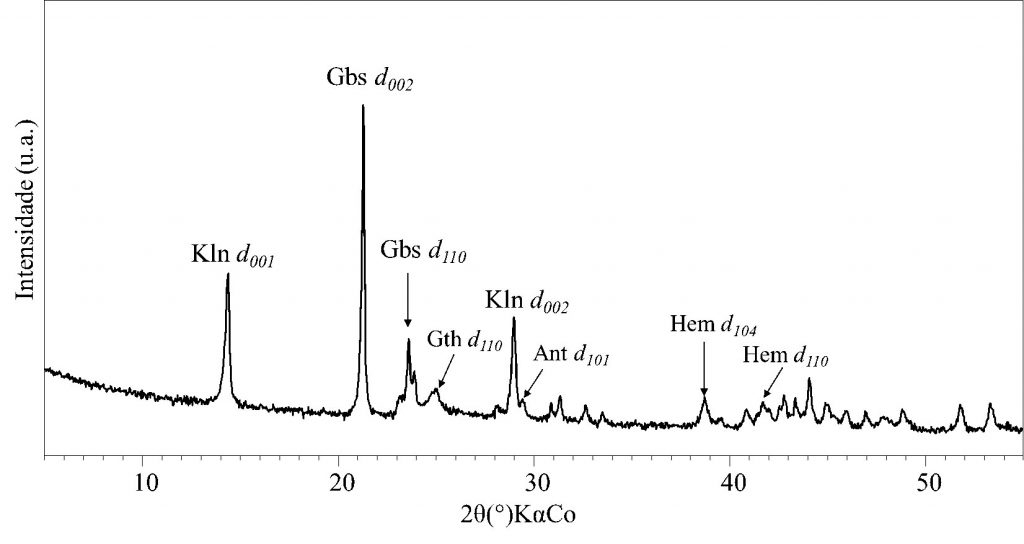
Figura – Difratograma de raios X do RGC (Kln: caulinita, Gbs: gibbsita, Gth: goethita, Ant: anatásio, Hem: hematita).
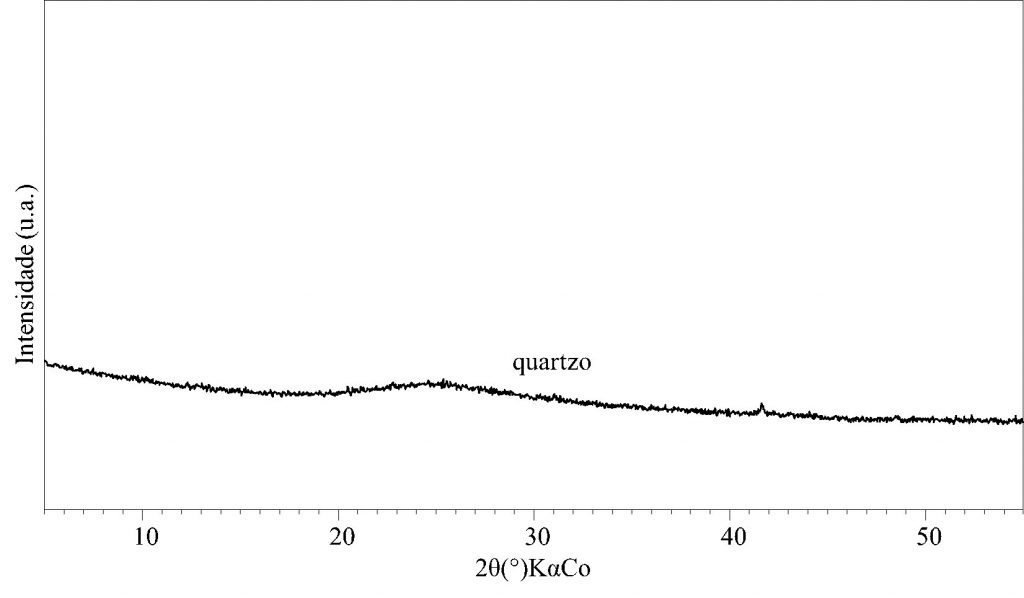
A Fig. 3 apresenta o resultado de DRX do coproduto silicoso SILMIX. Observa-se que o difratograma desta amostra é característico de um material amorfo, pois este não apresenta ordenamento cristalino (Kloprogge et al. 2002; Hildebrando et al., 2012), por isso não há a presença de minerais majoritários, apenas picos discretos em 3,34 Å, 4,25 Å e 2,45 Å, que são característicos do quartzo.
A composição química do RGC e SILMIX são apresentados na Tabela 4. Observa-se que a composição do RGC (% massa) é majoritariamente formada por SiO2 e Al2O3, totalizando mais de 60 % dos componentes. Tais constituintes, estão relacionados a presença dos minerais gibbsita e caulinita, os quais são as espécies químicas de maior interesse para síntese de zeólitas. O teor de ferro está relacionado a presença dos minerais hematita e Al-goethita, já o de titânio está relacionado à presença de anatásio. Observa-se na tabela 4 que o SILMIX tem como constituinte predominante o SiO2 com 95,3 %.
No trabalho desenvolvido por Santos et al. (2020), o percentual 21,8 % mostrado na Tabela 4, que corresponde a perda ao fogo (P.F.), está relacionado a perda de hidroxilas quando o material é submetido a altas temperaturas, devido a predominante presença dos minerais hidratados: gibbsita, caulinita e Al-goethita.
Tabela 4 – Composição química das amostras RGC e SILMIX.
| Amostras | constituintes (%) | |||||||
| SiO2 | Al2O3 | Fe2O3 | CaO | MgO | K2O | TiO2 | P.F. | |
| RGC | 18,4 | 45,1 | 12,9 | – | – | – | 1,8 | 21,8 |
| SILMIX | 95,3 | 0,3 | – | 0,7 | 0,6 | 0,6 | – | 2,5 |
Nota: (P.F.) perda ao fogo à 1000 ºC.
3.2 ANÁLISE DRX-CLUSTER DOS PRODUTOS
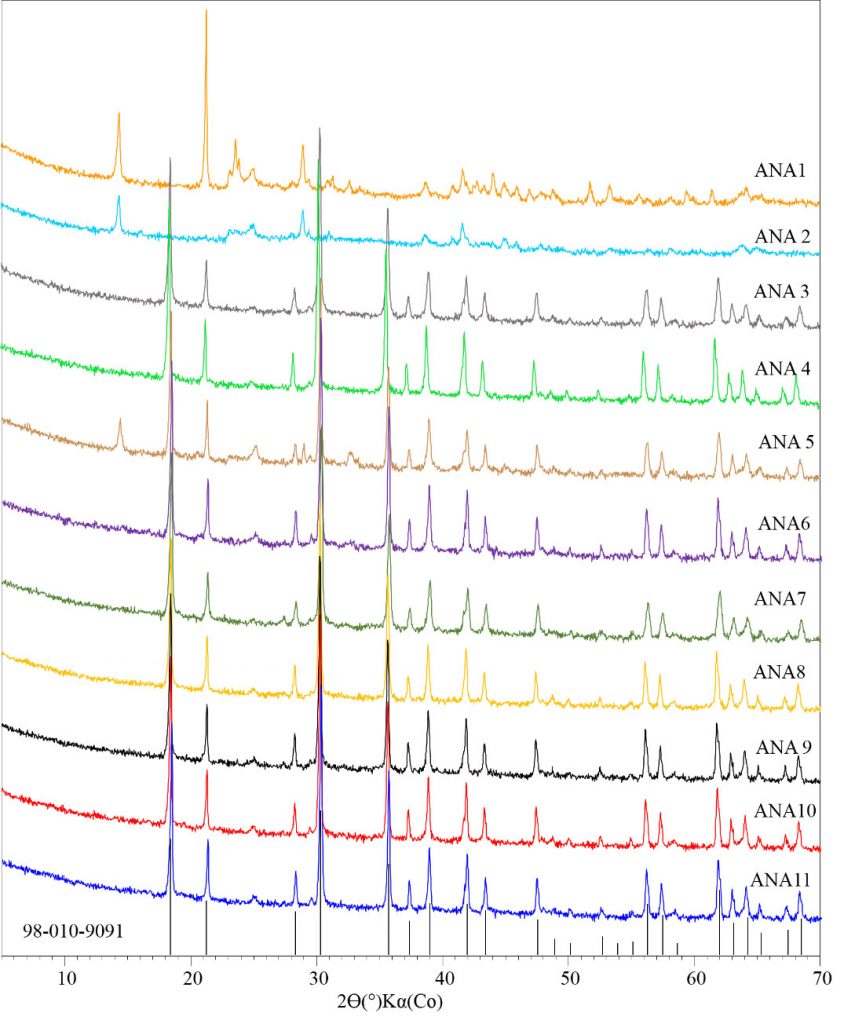
A Fig. 4 apresenta os 11 difratogramas de raios X dos produtos zeolíticos. As amostras foram comparadas com o padrão ICSD 98-010-9091, em que foi possível verificar que para a maioria dos ensaios a fase quase que exclusiva foi o mineral analcima (ANA).
Antes de qualquer análise estatística já é possível fazer inferências pela observação dos padrões difratométricos resultantes dos produtos: (i) os minerais fontes (caulinita e gibbsita) não foram completamente ou maximamente solubilizados sob a menor temperatura (110 °C) (ANA1, ANA2 e ANA5), exceto em combinação com a maior concentração de solução NaOH (3,5 mol.L-1) e maior tempo (48 horas) (ANA6); (ii) as réplicas executadas em ensaios aleatórios – ANA9, ANA10 e ANA11 – foram semelhantes e, portanto, reproduziram muito bem o experimento e (iii) a resposta da condição-combinação mediana (2,5 mol.L-1/145 °C/26 horas) foi semelhante as respostas das condições-combinações com níveis maiores. Ver também Tabela 5. Para García-Villén et al. (2018), o aumento do tempo levou ao desaparecimento da ANA, enquanto que as altas temperaturas entre 150 e 200 ºC favoreceram a cristalização.
Tabela 5 – Respostas para a matriz DOE completo 23.
| Ensaios | Variáveis Codificadas | Respostas (nºfótons difratados/s) | ||||
| Ordem Padrão | X1 | X2 | X3 | (d112) | (d004) | (d233) |
| ANA1(2) | – | – | – | 281 | 261 | 0 |
| ANA2(5) | + | – | – | 0 | 267 | 0 |
| ANA3(5) | – | + | – | 3463 | 4144 | 1899 |
| ANA4(4) | + | + | – | 4034 | 3775 | 2618 |
| ANA5(8) | – | – | + | 3059 | 4163 | 1579 |
| ANA6(10) | + | – | + | 3838 | 4685 | 2464 |
| ANA7(6) | – | + | + | 4143 | 5230 | 2119 |
| ANA8(7) | + | + | + | 3838 | 5490 | 2598 |
| ANA9(3) | 0 | 0 | 0 | 3733 | 5094 | 2415 |
| ANA10(9) | 0 | 0 | 0 | 4044 | 5745 | 2560 |
| ANA11(1) | 0 | 0 | 0 | 4116 | 4901 | 2173 |
(*) Ordem de ensaio
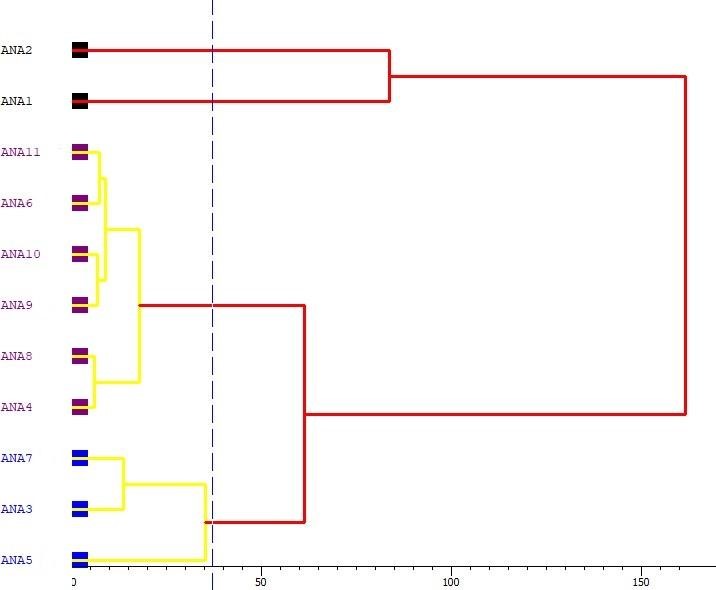
De acordo com as condições de agrupamento adotadas nesse trabalho, a análise de cluster revelou dois clusters e dois outliers (ANA1 e ANA2), ver dendograma na Fig. 5 e Análise de Componentes Principais 3D (PCA), na Fig. 6. Os outliers (amostras não agrupadas) podem ser explicados pelas características de pouca transformação dos materiais de partida em analcima; isto é, os ensaios com menor temperatura (110 ºC) e menor tempo (4 horas) não foram significativos para tal transformação, mesmo aumentado a concentração de 1,5 para 3,5 mol.L1, ANA1 e ANA2, respectivamente, ver Fig. 4.
O cluster 1 (azul) é o agrupamento dos produtos zeolíticos com a menor concentração (1,5 mol.L1), enquanto o cluster 2 (roxo) é aquele dos produtos com concentrações maiores, 2,5 e 3,5 mol.L1. Observa-se ainda que o cluster 2 é menos heterogêneo que o cluster 1, uma vez que apresenta menor distância euclidiana.
A triplicata dos pontos centrais (ANA9, ANA10 e ANA11), revelou uma boa execução dos ensaios e boa estabilidade do sistema experimental, pois as três réplicas pertencem ao mesmo cluster, mesmo os ensaios tendo sido executados de forma aleatória: terceiro, nono e primeiro, respectivamente.
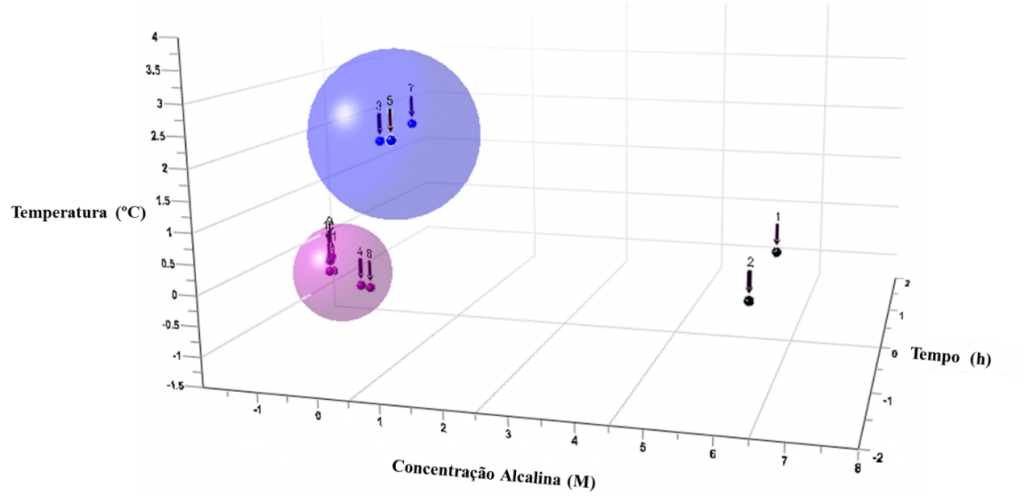
Figura 6 – Análise de Componentes Principais 3D (PCA): cluster 1 (azul), cluster 2 (roxo) e outliers (preto).
CONCLUSÕES
De acordo com os resultados apresentados neste trabalho, pode-se concluir que é possível produzir zeólita analcima como fase maximizada a partir de rejeito gibbsítico-caulinítico derivado do processo de lavagem do minério bauxita.
A análise DRX-cluster associada a um DOE completo 23 mostrou-se uma ferramenta prática e útil no estudo das variáveis de processo da síntese hidrotermal de Analcima, tornando possível otimizar uma região, condições de processo, para obtenção dessa zeólita a partir de RGC e SILMIX.
Inferindo uma análise sobre a obtenção do produto pretendido, segundo as condições ótimas e mais econômicas, concluiu-se que essas são: concentração de solução NaOH de 2,5M; temperatura de 145 ºC e tempo de 26 horas.
REFERÊNCIAS
Angélica, R.S.; Kahn, H.; Paz, S.P.A. 2018. A proposal for bauxite quality control using the combined Rietveld – Le Bail – Internal Standard PXRD method – Part 2: Application to a gibbsitic bauxite from the Paragominas region, northern Brazil. Minerals Engineering, 122, 148–155. DOI:10.1016/j.mineng.2018.03.039
Baerlocher, C.; Meier, W.M.; Olson, D.H. 2001. Atlas of zeolite framework, 5th ed., Elsevier.
Bernardi, A.C.C.; Werneck, C.G.; Haim, P.G.; Rezende, N.G.A.M.; Paiva, P.R.P.; Monte, M.B.M; 2008. Crescimento e nutrição mineral do porta-enxerto limoeiro ‘Cravo’ cultivado em substrato com zeólita enriquecida com NPK. Revista Brasileira de Fruticultura 30, 794-800. DOI: 10.1590/S0100-29452008000300039.
Bernardi, A.C.C.; Mendonça, F.C.; Werneck, C.G.; Haim, P.G.; Monte, M.B.M. 2009a. Disponibilidade de água e produção de arroz em função das doses de concentrado zeolítico. Irriga 14, 123-134.
Bernardi, A.C.C.; Monte, M.B.M; Paiva, P.R.P.; Werneck, C.G.; Haim, P.G.; Souza-Barros, F. 2009b. Produção de matéria seca e acúmulo de nutrientes após cultivos sucessivos com alface, tomate, arroz e capim andropogon em substrato com zeólita. Revista Brasileira de Ciência do Solo 33 (in press). DOI: 10.1590/S0100-06832010000200017.
Box, G.E.P.; Hunter, J.S.; Hunter, W.G. 2005. Statistics for Experimenters: Design, Innovation, and Discovery. 2ª ed. New Jersey: Wiley, 655 p.
Bortolini, H.R.: Lima, D.S.; Perez-Lopez O.W. 2020. Hydrothermal synthesis of analcime without template. Journal of Crystal Growth, Volume 532, 125424. DOI: 10.1016/j.jcrysgro.2019.125424.
BRASIL. 2018. Departamento Nacional de Produção Mineral <http://www.dnpm.gov.br /dnpm/sumarios/sumario-mineral-2018> acessado em 01 de junho de 2022.
Butler, B.M.; Palarea-Albaladejo, P.; Shepherd, K.D.: Nyambura, K.M.; Towett, E.K.; Sila, M.A.; Hillier, S. 2020. Mineral–nutrient relationships in African soils assessed using cluster analysis of X-ray powder diffraction patterns and compositional methods. Geoderma, Volume 375. DOI: 10.1016/j.geoderma.2020.114474.
García-Villén, F.; Flores-Ruíz, E.; Verdugo-Escamilla, C.; Huertas, F.J. 2018. Hydrothermal synthesis of zeolites using sanitary ware waste as a raw material, Appl. Clay Sci. 160, 238-248, DOI: 10.1016/j.clay.2018.02.004.
Hildebrando, E.A.; Angélica, R.S.; Neves, R.F.; Valenzuela-Diaz F.R. 2012. Synthesis of faujasite-type zeolite from kaolin waste. Cerâmica, 58, 453-458.
Jin, Y.; Liu, Z.; Han, L.; Zhang, Y.; Li, L.; Zhu, S.; Wang, D. 2022. Synthesis of coal-analcime composite from coal gangue and its adsorption performance on heavy metal ions. Journal of Hazardous Materials, 423, 127027. DOI:10.1016/j.jhazmat.2021.127027.
Kloprogge, J.T.; Hammond, M.; Hickey, L.; Frost, R.L. 2002. Low temperature synthesis of cobalt clays. Journal of Material Science Letters, v 21 p. 931-933. DOI: 10.1023/A:1016069505772.
Luz, A.B. 1995. Zeólitas: propriedades e usos industriais. 1. ed. Rio de Janeiro: CETEM/CNPq, 1995.
Maia, A.A.B.; Saldanha, E.; Angélica, R.S.; Souza, C.A.; Neves, R.F. 2007. Utilização de rejeito de caulim da Amazônia na síntese da zeólita A. Cerâmica, v. 53, p. 319-324.
Melo, C.C.A.; Melo B.L.S; Angélica, R.S.; Paz, S.P.A. 2019. Gibbsite-kaolinite waste from bauxite beneficiation to obtain FAU zeolite: Synthesis optimization using a factorial design of experiments and response surface methodology. Applied Clay Science, p. 125-134. DOI: 10.1016/j.clay.2019.01.010.
Melo, C.C.A.; Oliveira, K.S.; Angélica, R.S.; Paz, S.P.A. 2017. Análise de agrupamentos associada a difratometria de raios‐X: uma classificação mineralógica prática de bauxitas e seus produtos de digestão Bayer. Holos, 6, 32-42. DOI: 10.15628/holos.2017.6387.
Mencía, R. V. de la V.; Goiti, E.; Ocejo, M.; Giménez, R.G. 2019. Synthesis of zeolite type analcime from industrial wastes. Microporous and Mesoporous Materials, Volume 293, 109817. DOI:10.1016/j.micromeso.2019.109817.
Menezes, R.A.; Paz, S.P.A.; Angélica, R.S.; Neves, R.F.; Neumann, R.; Faulstich, F.R.L.; Pergher, S.B.C. 2017. Synthesis of ultramarine pigments from Na-A zeolite derived from kaolin waste from the Amazon, Clay Miner. 52 (1) 83–95, https://doi.org/ 10.1180/claymin.2017.052.1.06. DOI: 10.1180/claymin.2017.052.1.06.
Montgomery, C.D. 2008. Design and Analysis of Experiments. 7ª ed. New Jersey: Wiley.
Moraes, C.G.; Rodrigues, E.C.; Angélica R. S.; Macêdo, E.N.; Neves, R.F. 2013. Analcime zeolite production from amazon kaolin. Cerâmica, volume 59, 563-569. DOI:10.1590/S0366-69132013000400012.
Nascimento, L.G.; Paz, S.P.A.; Angélica, R.S.; Kahn, H. 2013. 57º congresso brasileiro de cerâmica 5º congresso iberoamericano de cerâmica. In: Síntese de Zeólitas a Partir Do Rejeito Gibbsítico/Caulinítico Do Beneficiamento de Bauxita de Paragominas-PA, p. 1019–1029.
Paz, S.P.A.; Angélica, R.S.; Neves, R.F. 2010. Síntese hidrotermal de sodalita básica a partir de um rejeito de caulim termicamente ativado. Química Nova, v.33, n.3, p. 579-583. DOI: 10.1590/S0100-40422010000300017.
Paz, S.P.A. 2016. Desenvolvimento e otimização de métodos de controle de qualidade e de processo de beneficiamento para bauxitas gibbsíticas tipo-Paragominas. Ph.D. Thesis, Universidade de São Paulo.
Paz, S.P.A; Angélica, R.S.; Kahn, H. 2017a. Optimization of the reactive silica quantification method applied to Paragominas-type gibbsitic bauxites. International Journal of Mineral Processing 162, 48–57. DOI: 10.1016/j.minpro.2017.03.003.
Paz, S.P.A.; Torres, P.W.T.S.; Angélica, R.S.; Kahn, H. 2017b. Synthesis, Rietveld refinement and DSC analysis of Al-goethites to support mineralogical quantification of gibbsitic bauxites. J Therm Anal Calorim 128, 841–854. DOI: 10.1007/s10973-016-5987-4.
Paz, S.P.A.; Kahn, H.; Angélica, R.S. 2018. A proposal for bauxite quality control using the combined Rietveld – Le Bail – Internal Standard PXRD method – part 1: hkl model developed for kaolinite. Minerals Engineering 118, 52–61. DOI: 10.1016/j.mineng.2018.01.006
Pinheiro, D.R., Paz, S.P.A.; Neves, R.F. 2021. A sequential Box-Behnken Design (BBD) and Response Surface Methodology (RSM) to optimize SAPO-34 synthesis from kaolin waste. Microporous and Mesoporous Materials, Volume 323. DOI: 10.1016/j.micromeso.2021.111250.
Saldanha, E. 2007. Síntese e caracterização da analcima a partir de rejeito de caulim e aplicação como adsorvente. Dissertação de Mestrado em Engenharia Química apresentado ao Centro Tecnológico da Universidade Federal do Pará. Belém, 2007.
Santos, L.G.S; Paz, S.P.A.; Cunha, E.J.S.; Souza, J.A.S. 2020. Non-halogenated flame-retardant additive from Amazon mineral waste. Journal of Materials Research and Technology. Volume 9, Issue 5, p. 11531-11544. DOI: 10.1016/j.jmrt.2020.08.007.